Информационная справка о коллаборации Синовак и АО ЛЕКХИМ касательно профилактической вакцины против вируса SARS-CoV-2, вызывающего болезнь COVID-19
Коротко:
- АО ЛЕКХИМ и Синовак подписали эксклюзивное дистрибьютерское соглашение.
- Синовак успешно завершил клинические испытания I и II фазы в Китае и начал испытания III фазы в Бразилии на большой выборке добровольцев из группы риска.
- После завершения исследований III фазы вакцина может быть зарегистрирована в Украине
- АО ЛЕКХИМ планирует начать поставки вакцины в Украину в декабре 2020 – январе 2021 года
Введение
Согласно данным Всемирной Организации Здравоохранения на 27/07/2020 из 164 разрабатываемых вакцин-кандидатов только 5 вышли на III фазу клинических исследований (3 китайских, 1 европейская и 1 американская). Именно III фаза клинических испытаний является решающей. В I и II фазах оценивают только безопасность и иммуногенность (способность вызывать иммунный ответ). Третья фаза проводится уже на большой выборке добровольцев из группы риска и напрямую оценивает эффективность вакцины – то есть способность противостоять вирусу.
Производитель вакцины-кандидата
Синовак (Sinovac Biotech) – крупнейшая китайская компания по производству вакцин, основанная в Пекине в 2001 году, производит от 300 до 500 млн доз вакцин в год. Синоваком были разработаны и выведены на рынок вакцины против Гепатита А и А+В, вирусов Гриппа, включая птичий, паротита. Синовак является акционерной компанией. Акции компании котируются на американской фондовой бирже NASDAQ.
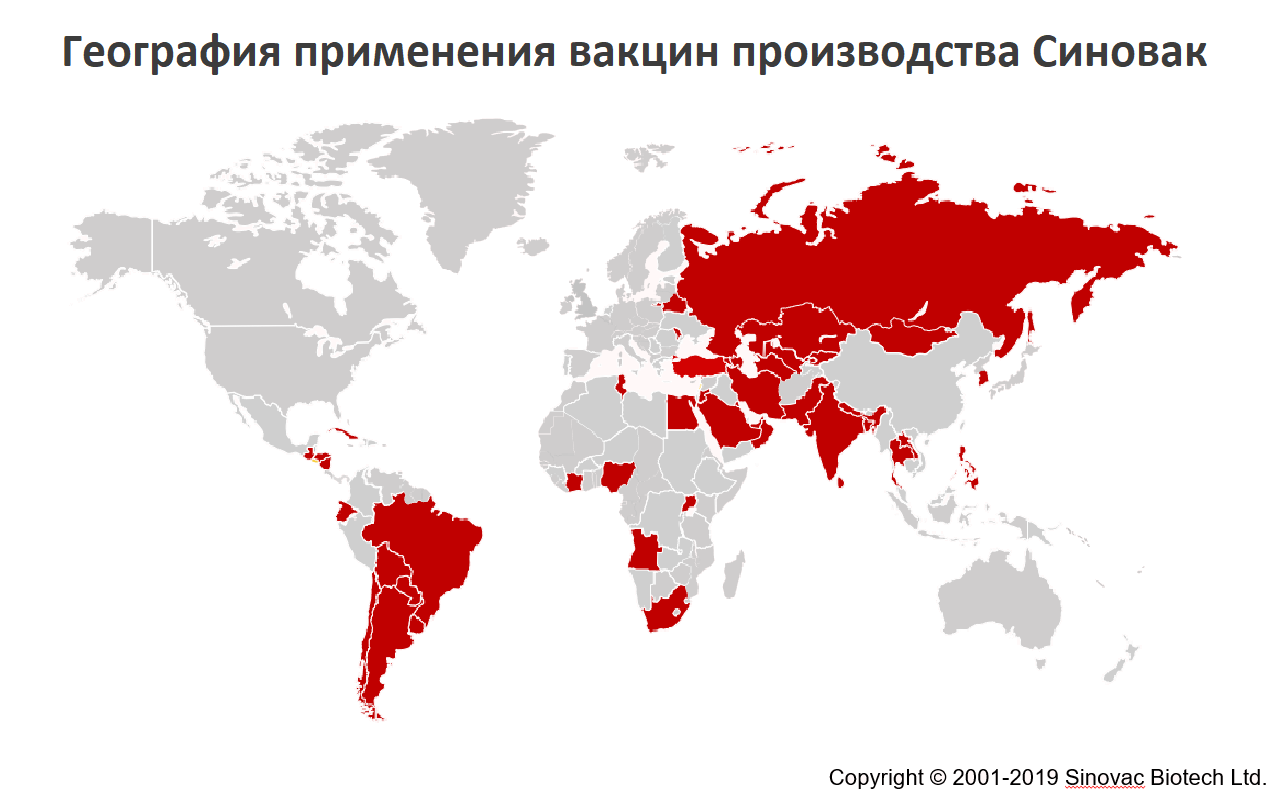
Вакцины Синовак одобрены в 34 странах мира, включая такие страны как Аргентина, Бразилия, Индия, Турция. Вакцина против Гепатита А является преквалифицированной Всемирной Организацией Здравоохранения.
За время существования компании, c 2002 было осуществлено более 3 миллиардов вакцинаций, 59 миллионов из которых у детей.

Разработка Вакцины COVID-19
В 2004 Синовак успешно завершил разработку, доклинические и первую, вторую фазу клинических испытаний вакцины против вируса SARS-CoV (первого типа). Эти наработки позволили быстро приступить к созданию вакцины против родственного вируса SARS-CoV-2, вызывающего болезнь COVID-19.
Вакцина объединяет устойчивость к различным штаммам SARS-CoV-2. При разработке были использованы 12 различных штаммов из Китая, Италии, Испании, Швейцарии, Германии, Великобритании.
Лекарственная форма: инактивированные вирусные частицы со стабилизатором
Способ дозирования: 2 дозы внутримышечно в верхнюю часть руки с интервалом 2-недели
На сегодняшний день, за этой разработкой и ходом клинических испытаний вакцины-кандидата, с Синоваком сотрудничает ВОЗ, Европейский Союз, US FDA, Аргентина, Бразилия, Индонезия, и другие страны, в которых будут так же проводить клинические исследования.

Проведенные исследования
-
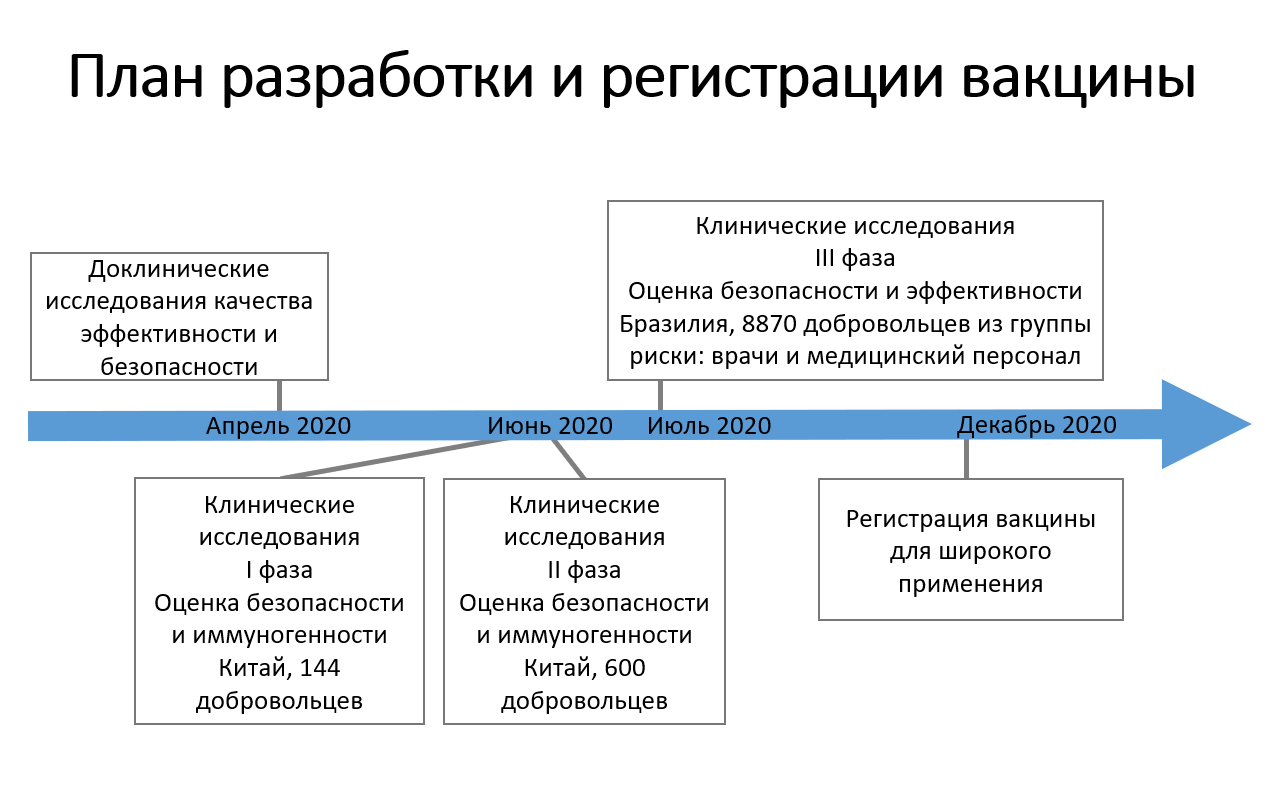
Доклинические исследования безопасности (острой, хронической и специфической токсичности и местной переносимости) и эффективности (иммуногенность, контрольное заражение, перекрёстный иммунитет к различным штаммам), включая исследования на приматах (макака резус и макака яванская). Подтверждена безопасность и выполнен предварительный подбор доз и режим дозирования.
-
Клинические исследования Фаза I в Китае – апрель-июнь 2020 – 144 добровольцев, 2 уровня доз, 2 режима дозирования. Показана безопасность вакцины и предварительно оценена эффективность (иммуногенность).
-
Клинические исследования Фаза II в Китае – май-июнь 2020 – 600 добровольцев, 2 уровня доз, 2 режима дозирования. Обработка данных завершена. Показана безопасность вакцины и оценена эффективность (иммуногенность), выбрана дозировка и режим дозирования.
Текущие исследования
-
Клинические исследования Фаза III в Бразилии, начаты в июле 2020 – 8870 добровольцев-медиков и з группы риска. Основные цели исследования: прямая оценка эффективности по частоте случаев заболевания в течении 2 недель после получения второй доз вакцины и частота побочных реакций 7 дней после каждой иммунизации. Исследование проводится Институтом Бутантан, который подчиняется Секретариату здравоохранения штата Сан-Паулу (Бразилия).
Благодаря заблаговременно начатому сотрудничеству и большой подготовительной работе, АО ЛЕКХИМ планирует приступить к регистрации вакцины Синовак сразу по завершению исследований в Бразилии. Кроме того, полгода совместной работы над проектом убедили нас, что Синовак заинтересован вывести на рынок качественный и хорошо изученный продукт.
АО ЛЕКХИМ понимает всю важность поставок вакцины для восстановления жизнедеятельности страны.
